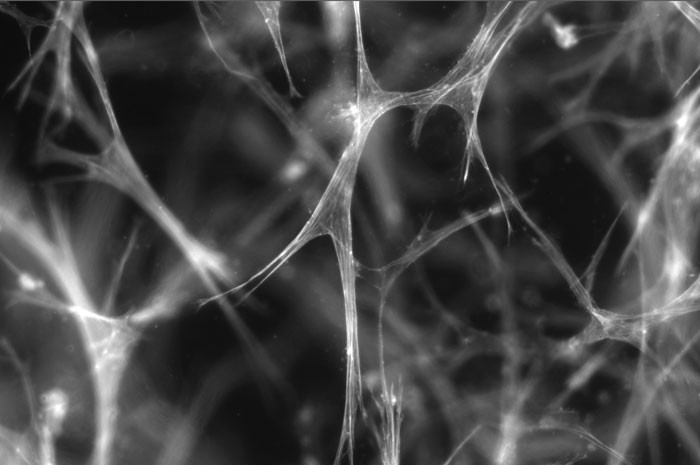
Cellules musculaires lisses en croissance dans une matrice de collagène en 3 dimensions. La photo montre que les cellules sont bien établies au sein de la matrice et qu’elles créent des connexions avec leurs voisines. Cela prouve qu’elles poussent bien et qu’elles tentent de recréer leur environnement, comme dans le corps humain.La photo présente l’intérieur d’un gel de collagène colonisé par les cellules musculaires lisses.
L’histoire
Dans les pays industrialisés, on meurt d’abord du cœur, et, dans le monde, 18 millions de personnes décèdent chaque année en raison de vaisseaux sanguins obstrués. Tristement, cette pathologie, l’athérosclérose, connaît de « beaux » jours avec l’obésité, l’hypertension, le tabagisme et l’allongement de la durée de vie. Malgré d’importants progrès, les techniques curatives actuelles, telle la pose de stents (treillis métalliques soutenant la paroi de l’artère tout en rétablissant la circulation sanguine), ne suffisent pas.
Peut-on remplacer les vaisseaux engorgés? Certainement. Parmi les approches possibles se trouve celle consistant à faire croître dans une éponge de collagène des « artères » en 3D.
L’ingénierie tissulaire
À partir des années 1980, les chercheurs ont partagé leurs savoir-faire dans les domaines de la médecine, de la biologie et des sciences des matériaux afin de développer des structures colonisables par les cellules tout en étant implantables. Ce fut l’émergence de l’ingénierie tissulaire.
L’ingénierie des tissus vasculaires pourrait non seulement fournir des substituts aux vaisseaux naturels, mais aussi rendre la clé des champs aux animaux de laboratoire. De fait, pendant que le chirurgien remplacerait les vaisseaux endommagés des patients, les chercheurs pourraient étudier la maladie et tester de nouveaux médicaments tout en diminuant l’expérimentation animale.
Le système vasculaire
Une artère est un tissu complexe avec une architecture bien précise, qui comporte trois couches appelées « tuniques ».
À l’intérieur, en contact avec le sang, se trouve l’intima. Elle est composée d’une monocouche de cellules endothéliales.
La couche intermédiaire, la média, joue un rôle central dans la régulation de la circulation. C’est la tunique la plus épaisse des artères, celle qui doit être plus résistante et plus élastique que les veines afin d’assurer la vasomotricité du vaisseau sanguin. Elle comprend des cellules musculaires lisses disposées en anneaux enchevêtrés dans une matrice faite en partie d’élastine et de collagène. C’est grâce à ce muscle lisse que se produisent la vasodilatation (augmentation du calibre due au relâchement des cellules) ou la vasoconstriction (réduction du calibre due à la contraction des cellules). De légères variations du diamètre des vaisseaux ont des effets marqués sur le débit ou la pression du sang.
La couche externe est l’adventice. Elle est composée de fibres de collagène lâchement entrelacées, de quelques fibres élastiques et de fibroblastes. Les fibres permettent aux vaisseaux sanguins de s’étirer tout en empêchant une trop grande dilatation. Cette tunique sert d’ancrage au tissu environnant.
La recherche
La culture cellulaire s'effectue dans des flacons spécifiques où un seul type de cellules croît en deux dimensions, « en tapis », et ce, jusqu’à confluence. L’épaisseur de la culture est négligeable par rapport à son étendue.
Nos organes, eux, sont en trois dimensions et, de plus, ils sont composés de nombreux types de cellules. Pour fabriquer un nouveau tissu vivant, il est nécessaire de faire de la culture cellulaire en 3D. Pour cela, il faut un support appelé « échafaudage ».
Le Laboratoire de biomatériaux et bioingénierie de l'Université Laval a sélectionné le collagène comme support de base pour soutenir et favoriser la régénération des tissus vasculaires. Le collagène, naturel, est couramment utilisé en raison de ses excellentes propriétés biologiques qui lui confèrent un fort potentiel pour appuyer et guider le processus de régénération cellulaire et tissulaire. De fait, le collagène est le principal composant de la plupart des tissus conjonctifs (la peau, les os, le cartilage, les artères) des mammifères. On le retrouve aussi dans la composition des artères, et il représente environ 25 % de toutes les protéines du corps.
Le collagène est extrait au laboratoire à partir du tendon de la queue de rat, puis transformé en éponge. Les éponges peuvent être conservées pendant plusieurs mois à -80 °C. Quand nous avons besoin de collagène, nous solubilisons les éponges dans de l’acide acétique, puis la solution est stérilisée.
L’approche
L’approche privilégiée consiste à reproduire d'abord la média, car elle fournit les propriétés élastiques à la paroi de l’artère et joue un rôle essentiel dans le transport du sang. Nous isolons les cellules musculaires lisses depuis les artères de cordons ombilicaux récupérés après accouchement, avec l’accord d’un comité d’éthique et le consentement unanime des parents. Ces cellules sont mélangées avec la solution de collagène et une solution tampon qui permet de ramener le pH de la solution finale à 7. Le mélange est ensuite coulé dans un moule (tube avec mandrin pour mimer une artère, ou simplement dans une boite de Petri pour former des disques) et placé à 37 °C, la température favorable à la croissance des cellules. Après quelques heures, le collagène est gélifié, et les cellules poussent ainsi dans une matrice en trois dimensions, ce qui est fort semblable à ce qui se produit chez le fœtus à la phase de génération de tissus vasculaires et lors de la régénération des tissus matures du corps humain.
- Caroline Loy
Université Laval
Caroline Loy a une formation en biologie cellulaire et en physiologie, qu’elle a approfondie avec un master en ingénierie biomédicale effectué en France. Elle est actuellement étudiante au doctorat au Laboratoire de biomatériaux et de bioingénierie de l’Université Laval de Québec sous la supervision du professeur Diego Mantovani, titulaire de la Chaire de recherche du Canada Tier I pour l’innovation en chirurgie. Ses travaux de recherche visent à concevoir, développer et valider un système de coculture favorisant la régénération du tissu vasculaire. Ils sont réalisés en collaboration avec le professeur Jayachandran Kizhakkedathu de l’Université de Colombie-Britannique à Vancouver.
Vous aimez cet article?
Soutenez l’importance de la recherche en devenant membre de l’Acfas.
Devenir membre




